A termodinamika kivételes fizikai elmélet. Célkitûzése a makroszkopikus testek energiacserével járó folyamatainak jellemzése. Eredetileg ezt a célt a belsõ szerkezetre, a mikroszkopikus szabadsági fokokra történõ bármiféle utalás nélkül kívánja elérni. Ennek köszönhetõ eredményei alkalmazhatóságának széles tartománya, univerzalitása. Sok esetben meglepõen erõs megszorítást jelentõ következtetések nyerhetõk módszereivel a mikroszkopikus szerkezetre is. Alapegyenlete valamely egyszerû mechanikai rendszer és környezete között kvázisztatikusan zajló energiacserélõ folyamatok során az egyszerû rendszerben bekövetkezõ állapotváltozást korlátozó összefüggést fogalmazza meg:
A kvázisztatikus hõcsere egyenletének integrálásával meghatározható egy folyamatfüggetlen, valamint a mechanikai és elektromágneses állapothatározóktól is független makroszkopikus állapothatározó, az entrópia:
Ennek integrációs állandóját a harmadik fõtétel nullára rögzíti az abszolút hõmérsékleti skála nullapontjában.
A termodinamika a nem-redukcionista (azaz a jelenségeket kisebb alkotórészek közötti folyamatokra visszavezetni nem kívánó) fizika nagyszerû teljesítménye. A redukcionista megközelítéstõl való tartózkodás az az erény, amely egyéb, összetett nem-fizikai rendszerek (gazdaság, társadalmi szervezet stb.) kutatóit arra ösztönözte, hogy saját területükön analóg leírást keressenek, egyszerû szabadsági fokokat azonosítsanak, és egyenlõtlenség-alakú, változási irányt jelzõ összefüggésre jussanak. Megemlíthetõ Nicholas Georgescu- Roegen (2. kép ), aki 1971-ben publikálta Az entrópiatörvény és a gazdasági folyamat címû könyvét. Ez a könyv nagy hatással volt az ökológiai gazdaságtan irányzatának létrejöttére, amely a természeti és emberi erõforrásokkal létrehozható gazdasági értéket az erõforrások állapotának reprodukálása mellett kívánja optimalizálni.
A termodinamikusok mindmáig élénk vitája a termodinamika második fõtételéhez vezetõ axiómák pontos megfogalmazását, a törvény alá vetett folyamatok egyértelmû körülhatárolását célozza. Ebben a tisztázó folyamatban Max Planck is aktívan részt vett, többek között 1897-ben kiadott tankönyvével, valamint a termodinamika harmadik tételének és az abszolút hõmérséklet fogalmának elfogadtatásáért tett erõfeszítéseivel. Érdemes felfigyelni arra, hogy még élete végén írott tudományos életrajzában [1] is hangsúlyozza, hogy milyen nehézségbe ütközött a Carnot-ciklus levezetésére használt, a kalorikumelméletet tükrözõ eredeti vízimalom-hasonlatnak (3. kép ) kiszorítása a fizikusok gondolkodásából. A termodinamika redukcionista megközelítése a Ludwig Boltzmann által javasolt statisztikus mechanikai megalapozással jelentkezett, amelynek lényegét éppen Planck öntötte tömör, és a mechanikai rendszerekrõl továbblépõ általánosítást lehetõvé tevõ formába:
SN = kB ln WN,
ahol kB = 1,38 · 10-23 J/K. A kulcskérdés a WN mennyiség meghatározásának, azaz egy rendszer valamely rögzített belsõ energiájú makroállapotát megvalósító mikroállapotok leszámolásának mozzanata. Ez a lépés két kritikus kérdést hordoz magában. Az elsõ: az adott állapot szempontjából alapvetõnek tekinthetõ alkotórészek (szabadsági fokok) azonosítása. A második: a szabadsági fokok diszkretizálása, ami leszámlálhatóságuk elõfeltétele. A termodinamikus Planck sokáig kritikusan vélekedett a mechanika idõtükrözésre szimmetrikus törvényeit a valószínûségi megközelítéssel ötvözõ statisztikus mechanikai irányzat és a termodinamika összekapcsolhatóságáról. Szerepet játszott a molekuláris rendezetlenség kiegészítõ fogalmának kialakításában, amely a mechanika törvényein túllépõ feltétel a folyamatok idõirányának meghatározottságára vezetõ H-tétel alkalmazhatóságára. Tudományos felfogásában ezért igazi személyes fordulatnak tûnik, hogy az elektromágneses térrel termikus egyensúlyban lévõ abszolút fekete test sugárzási spektrumának értelmezéséhez a Boltzmann-féle valószínûségi entrópiafogalomra épülõ elméletet dolgozott ki. Ebben a jelenségben is, mint a termodinamika egész konstrukciójában, valószínûleg az univerzalitás ragadta meg. Ma ezt úgy fogalmazhatjuk, hogy a hõmérsékleti sugárzás spektruma független attól, hogy a laboratóriumban gondosan hõszigetelt, tükrözõ falú tartály belsejében elhelyezkedõ szénszemcse sugárzása, vagy a Világegyetem egészét kitöltõ elektromágneses állóhullámok valósítják-e meg.
E felismerés alapján Planck a végeredmény szempontjából közömbös modellrendszert választott: egyetlen, elektromosan töltött harmonikus oszcillátor kölcsönhatását vizsgálta az abszolút fekete testet megvalósító üregrezonátor elektromágneses állóhullámaival. Termodinamikusként eltért kortársai megközelítésétõl, amely közvetlenül az üreg/oszcillátor kis frekvenciatartománybeli energiasûrûségének meghatározására irányult. Tudván, hogy az entrópia a rögzített térfogatú rendszerben az energiának egyértelmû függvénye, N darab frekvenciájú oszcillátor halmazára érvényes entrópia-energia összefüggés megalkotását tûzte ki céljául. Boltzmann fenti képletét használta kiindulásul. A feladat N oszcillátor NE összenergiájú makroállapotához tartozó mikroszkopikus állapotok WN számának meghatározása volt. Erre irányuló próbálkozásai során, a leszámlálhatóság biztosítására folyamodott az energiakvantálás „kétségbeesett” feltevéséhez:
N E = Pε
. Itt ε a kvantált energiacsomag nagysága, P pedig a teljes energia csomagokba osztásával adódó csomagszám. Nagyon nagyszámú oszcillátorhoz nagyon nagy P érték kell. Ebben a határesetben Stirling képlete segítségével értékelte ki WN kombinatorikai képletét, amellyel eljutott az egyetlen oszcillátor entrópiájának képletéhez:
. Miután a termodinamikában az entrópiának a belsõ energia szerinti parciális deriváltja adja a T hõmérséklet reciprokát, a fenti képletbõl adódik
. Ebbõl azután kifejezhetõ az oszcillátor E belsõ energiája T hõmérsékleten, amit az oszcillátorok állapotsûrûségével megszorozva Planck megkapta a róla elnevezett sugárzási törvényt. (Hallgatólagosan persze feltette, hogy termikus egyensúlyban az oszcillátorral képviselt abszolút fekete test és az azt övezõ sugárzás energiája a spektrum minden vonalára egyezik.) A kapott összefüggésnek a Wien-törvénnyel való összevetése is szükséges még, ami végül megköveteli az energiakvantumra az
ε = h
arányosságot. Közismert, hogy Planck jelentõs, de hiábavaló erõfeszítést tett az energiakvantálási feltételtõl való megszabadulásra. Ez a törekvés érthetõ, hiszen a fentiek szerint õ pusztán a szabadsági fokok (a mikroállapotok) megszámlálhatósága érdekében diszkretizálta az oszcillátorhalmaz energiáját. Einstein és követõi a legkülönfélébb anyagi rendszerek elemi oszcillátorként viselkedõ szabadsági fokaira alkalmazták a kvantálás eljárását. A szilárd testek fajhõjétõl a fényingadozások statisztikájáig siker sikert követett. Az entrópia megszületésétõl a sugárzás entrópiájáig vezetõ, fél évszázadot átfogó történet összefoglalásául idézni kívánom Varró Sándor kommentárját [2], amelyet Max Plancknak az 1911-es Solvay-konferencián tartott elõadására alapozott: „Az energia kvantáltságának gondolata Boltzmann-nak 1872-ben és 1877- ben megjelent munkáira vezethetõ vissza. Bár Boltzmann pusztán matematikai eszköznek tekintette a diszkrét elemi energiacsomagokat, mégis második cikkében - amelyben elvégezte a (termodinamikai) valószínûség kombinatorikai elemzését és kiszámította annak maximumát, megkapta a gáz molekulái által hordozott energiacsomagok (Bose-)eloszlását. Planck megjegyezte, hogy a kombinatorikus megvalósítások teljes száma, illetve azok maximális valószínûséggel bekövetkezõ konfigurációinak száma között a különbség elhanyagolható lévén, Boltzmann eredménye egyezik az õ entrópiaképletével.”
Az Univerzum entrópiája és a fekete lyukak
Az Univerzum egészére érvényes, a gravitációt is magábafoglaló termodinamika lehetõségét sokan vitatják, ám Stefan és Boltzmann képletével, amelynek együtthatóját Planck sugárzási törvénye meghatározza, könnyen kiszámítható az egykor létezett termikus egyensúlyból lecsatolódott, azóta kölcsönhatásmentes ideális gázként hûlõ kozmikus fotonok és neutrínók által hordozott entrópia. A termodinamikai entrópia sûrûsége a hõmérséklet harmadik hatványával arányos. A 1028 cm méretû eseményhorizontunk belsejében 2,725 K hõmérsékletû fotongáz és 1,96 K hõmérsékletû neutrínógáz mindegyike az önmagában nehezen elképzelhetõ óriási nagyságrendet képviselõ 1088 entrópiát hordozza (k egységben számolva!). A gravitációs energia hipotetikus kvantumai jóval korábban csatolódtak le, egyensúlyi gázuk ezért kisebb, 1086 entrópiát hordozhat. Amennyiben nem állt fent termikus egyensúly a lecsatolódásuk pillanatában, akkor entrópiájuk e becslésnél kisebb. Az Univerzumban található nem-relativisztikus állapotú, elektromágneses sugárzást kibocsátó anyag entrópiája az anyag-antianyag aszimmetria értéke alapján becsülhetõ meg. Ezt az információt elõször a könnyû elemek õsszintézisének elméletébõl nyerhetõ kozmikus elõfordulási gyakoriságoknak a csillagászati mérésekkel való összevetésébõl sikerült kihámozni. Értéke érzékenyen befolyásolja a kozmikus háttérsugárzás észleléseit is, így ma legpontosabban a háttérsugárzási mérésekbõl ismert a nem-relativisztikus anyagsûrûségnek a háttérsugárzás entrópiájához viszonyított értéke: N(anyag)/S (foton ) ≈ 10-9. Az entrópiának az anyagmennyiséggel való arányossága (extenzivitása) miatt S (anyag) ≈ 1079. Az Univerzum energiasûrûségét domináló sötét anyag és sötét energia entrópiatartalmáról egyelõre nincs információ. Annyit tudunk, hogy a sötét anyag mennyisége nagyjából hatszorosa a világítani képesnek. Amennyiben nem-relativisztikus nehéz elemi részek alkotják, amint azt a szuperszimmetrikus világra vonatkozó elméleti konstrukciók sugallják, akkor entrópiatartalma legfeljebb egy-két nagyságrenddel lehet nagyobb az elektromágnesesen világító anyagénál. A sötét energia gravitációs hatását mai ismereteink szerint teljesen jól leírja a nem-zérus kozmológiai állandó feltételezése. Miután ebben az állandóban feltevés szerint nincs statisztikai viselkedés, entrópiája zérus. Az utóbbi két kategória természetének részletesebb megismerése entrópiatartalmukat illetõen is jelentõs módosulásokat eredményezhet. Mindezek a becslések a forró Univerzumban egykor fennálló termodinamikai egyensúlyból kiinduló termikus történethez kapcsolódnak. A statisztikus Boltzmann-definíció egy kiterjesztését használva azonban az entrópia fogalmat az 1970-es években sikerült alapvetõen általánosítani. Az alább ismertetendõ fejlemények alapján ma úgy tûnik, hogy az Univerzumban a szupermasszív fekete lyukak entrópiatartalma a meghatározó. Jacob Bekenstein (4. kép bal oldalán) 1973-ban, 26 éves korában írta meg tudománytörténeti jelentõségû Black Holes and Entropy címû cikkét [3]. A hagyományos termodinamika keretei között fekete lyukakhoz kapcsolható entrópiaparadoxonra J.A. Wheeler (4. kép jobb oldalán) figyelt fel, és Bekenstein számára PhD-témának adta a kérdéskört. Meg kellett értenie, hogy hová lesz a fekete lyukba behulló anyag entrópiája. Bekenstein Hawking munkáját használta kiindulásként, aki általános tétel szintjére emelte Wheeler másik diákjának, Christodoulou nak bizonyos, az egzakt fekete lyuk megoldások fejlõdésére vonatkozó észrevételét. Hawking tétele szerint a fekete lyuk eseményhorizontja felületének területe bármely folyamatban csak nõhet (az eseményhorizonton belülrõl induló fényjelek véges idõ alatt nem jutnak ki a külvilágba). Például két fekete lyuk összeolvadásakor a létrejövõ állandósult állapotú objektum (eseményhorizontjának) felülete nem lehet kisebb a két kiinduló fekete lyuk (eseményhorizontjai) felületének összegénél. Bekenstein cikke bevezetésében megjegyzi, hogy „mindez a termodinamika második tételére emlékeztet ...., a hasonlóság alapján érdemes a fekete lyukak fizikáját termodinamikai szempontból vizsgálni”. Cikkében javaslatot tett a fekete lyukak entrópiájának és felületének arányos mennyiségként történõ azonosítására, és ezzel sikeresen általánosította a termodinamika második tételét a fekete lyukak részvételével zajló folyamatokra. Bekenstein entrópiaképlete a következõ:

ahol A a fekete lyuk eseményhorizontjának a felülete, c a fénysebesség, G a Newton-féle gravitációs állandó, h pedig a Planck-állandó. η dimenziótlan arányossági tényezõ. A kvantumosságot jellemzõ h állandó megjelenését az entrópia és a felület mértékegysége közötti átváltás indokolja. Ez az egyetlen univerzális természeti állandó, amely a jó dimenziót adja. Az ismeretlen η számegyütthatót Bekenstein a C.E. Shannon által bevezetett I informatikai entrópiára támaszkodva becsülte meg, amelynek definíciója

Itt pn a vizsgált rendszer állapotai közül az n-ik megvalósulási valószínûsége. Egy bit információhoz ln2 informatikai entrópia társítható, ha a rendszert kétállapotúnak választva a két alternatív állapotról egyenlõ valószínûséget tételezünk fel. Bekenstein egyrészt megbecsülte egy pontszerû tömeg elnyelésénél bekövetkezõ felületnövekedés alsó korlátját, másrészt a horizont mögötti eltûnésével járó információcsökkenést ráérzéses alapon 1 bitnek választotta. A fekete lyuk entrópianövekedését az informatikai entrópiacsökkenéssel téve egyenlõvé jutott az közelítõ becslésre, amelynek egzakt értékét végül Hawking számolta ki. Szokás ezért Bekenstein-Hawking- entrópiát is emlegetni.
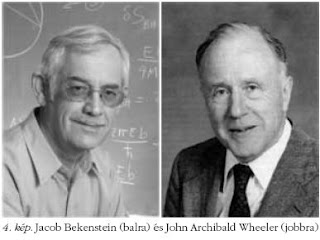
A fekete lyukakat az úgynevezett „kopaszsági tétel” miatt kisszámú makroszkopikus adatuk, azaz tömegük, elektromos össztöltésük, teljes impulzusmomentumuk kimerítõ mértékben jellemzi a külsõ megfigyelõ számára. Belsõ szerkezetükrõl semmiféle további információ nem nyerhetõ, például teljesen érdektelen, hogy adott tömegû fekete lyuk milyen folyamat eredményeképpen alakult ki, eseményhorizontjának belsejében a különféle töltésjellegû mennyiségek hogyan oszlanak el. Bekenstein javaslata szerint entrópiájuk mintegy a belsõ szerkezetre vonatkozó információ hiányának mértékét adja meg. Cikkében több, részletesen elemezhetõ példán mutatta meg, hogy egy fekete lyukba behulló, a tömegpontnál bonyolultabb, de még mindig igen egyszerû fizikai rendszer (pl. egy harmonikus oszcillátor) a teljes rendszer (fekete lyuk + oszcillátor) általánosított entrópiájának növekedését eredményezi. Az egyensúly fennállására vonatkozóan semmiféle elõfeltevést nem tett. A hagyományos és a fekete lyukakra bevezetett új entrópia összegének változási irányára vonatkozó kijelentés az
általánosított második törvény. Kvázisztatikus tömegelnyelésre azon észrevétel alapján terjesztette ki a második fõtétel differenciális alakját, miszerint az ismert Schwarzschild-megoldásban a fekete lyuk eseményhorizontjának sugara arányos annak tömegével. Miután a tömeget belsõ energiaként értelmezte, a megváltozás energiamérlege azt diktálja, hogy
dMfekete lyuk = T dSfekete lyuk.
Ezzel viszont hõmérséklet is értelmezhetõ a fekete lyukakra. A Schwarzschild-megoldás szerint ugyanis egy nem-forgó fekete lyuk Bekenstein-entrópiája a tömeg négyzetével arányos. Ezért a fenti képlet alján a fekete lyuk Hawking-hõmérséklete annak tömegével fordított arányban változik.

Az egyensúlyi állapotot egy statisztikus mechanikai rendszerben a kezdeti állapottól független, univerzális eloszlású állapot jellemzi. Az egyensúlyból kitérített rendszerek tapasztalat szerint véges idõ alatt relaxálnak az egyensúlyi állapotba. Miután a fekete lyuk hõmérsékleti sugárzása egyensúlyi jellege miatt a korábbi (a lyukba való behullás elõtti) információt „elfelejti”, Hawking feltételezte, hogy az elemi kvantumfolyamatokra érvényes úgynevezett unitaritási tulajdonság (az együttes valószínûség megmaradása) sérül. Erre kötött fogadást
Kip Thorne-nal és
John Preskill - lel (
5. kép ) valamikor a hetvenes évek végén, amire még visszatérünk. A fekete lyukak elõfordulási gyakorisága és jellemzõ tömege alapján az általuk hordozott entrópiára könnyen kapható becslés. Csillagászati megfigyelések alapján gyanítható, hogy minden galaxismagban, akárcsak a mi galaxisunkban, egy szupermasszív, a Nap tömegének tízmilliószorosát tartalmazó fekete lyuk helyezkedik el. Az Univerzum belátható részében található galaxisok számát 10
11-re becsülik. Bekenstein képletét alkalmazva a fekete lyukak teljes entrópiájára az

becslés adható. Levonható a tanulság, hogy az ismert anyagi alkotórészeknek az entrópiához adott termikus járulékát a fekete lyukaknál figyelembe vett információvesztésbõl származó járulék sok nagyságrenddel felülmúlja. Felmerül a kérdés, egyáltalán van-e felsõ korlát az Univerzum entrópiájára?
Hologram a világ!(?)
Világunk fundamentális alkotóelemeit a kvantumtérelmélet háromdimenziós ráccsal modellezi, amelynek rácspontjaihoz, illetve a szomszédos rácspontokat összekötõ élekhez társítja az önálló, bár egymással kölcsönható, szabadsági fokokat. A rácspontok távolságát az lPlanck Planck-hosszal becsülhetjük; az ennél kisebb hosszúságnak egyszerûen nincs értelme, hiszen a hosszúság a gravitáció által meghatározott téridõ- metrika része, és ez alatt a hosszúság alatt a kvantumingadozások szétkenik a klasszikus téridõ-geometriát. A Planck-hosszúság 10-35 m. Egy szabadsági fok állapotának ismeretéhez 1 bit információt rendelve a látható Világegyetem V térfogatának (kB egységben számolt) Boltzmann-Shannon-entrópiájára

becslés adható. g* az egy rácsponthoz tartozó szabadsági fokok száma. Ez a részecskefizika Standard modellje szerint nagyjából száz körüli szám. Ezzel a megközelítéssel az Univerzum informatikai entrópiáját 10192-re becsülnénk. A szuperszimmetrikus sötét anyaggal kiegészített elmélet legfeljebb egy nagyságrenddel növelheti meg ezt a becslést. Bekenstein 1994-ben felhívta a figyelmet arra, hogy valamely térrészben növelve az ott koncentrált energiát (az elemi részek nyelvén: a részecskesûrûséget) elérünk egy határt, amikor a tartomány fent vázolt térelméleti leírása értelmét veszti, mert a térrész fekete lyukká alakul [4]. A következõ gondolatkísérletet elemezte: Képzeljünk el egy tértartományt, amelynek entrópiája nagyobb, mint az ahhoz a térrészhez tartozó fekete lyuké. Ha nincs ott egy fekete lyuk, akkor fel kell tételeznünk, hogy azért nincs, mert kisebb energiával (tömeggel) rendelkezõ állapot valósul meg. Kezdjünk ezután tömeget adni ehhez a tartományhoz. (Ezt a gondolatkísérletet szokás Susskind-folyamatnak is hívni a javaslattevõ stanfordi fizikus neve után.) A tömeghatárt elérve megtörténik a feketelyuk- képzõdés, de a végállapot entrópiája kisebb, mint a kiinduló állapoté. Ez a folyamat sértené az általánosított entrópia növekedésének elvét. A konklúzió az, hogy egy V = 4πR3/3 térfogatú tértartomány tetszõleges állapotának maximális entrópiáját a térfogatot elfoglalni képes A = 4πR2 felületû eseményhorizonttal rendelkezõ fekete lyuknak megfelelõ

képlettel lehet megbecsülni. A Világegyetem maximális entrópiájára ezzel 10
126 adódik. Ehhez képest az ismert anyagformák termikus entrópiája elhanyagolható. Erre
R. Boussonak az elõzõhöz hasonló alakra hozott becslése világít rá a legtisztábban. Egy
R sugarú tartományban a relativisztikus részecskékkel társított entrópiára és energiára fennállnak az
S ≈ R3 T3, E ≈ R3 T4
arányosságok. Miután az energia nagyságát korlátozza a fekete lyuk kialakulásának esélye:
E ≤ állandó · R
ezért a relativisztikus részecskék gázának hõmérsékletére adódik a
T ≤ állandó · R-1/2
nagyságrendi korlát. Itt az állandó tényezõk konkrét értéke érdektelen, mivel csak a geometriai méretektõl való függés jellegét kívánjuk megérteni. Ezt az entrópiatartalom képletébe helyettesítve látható, hogy
S ≤ állandó ·
R3/2 ≈
A3/4
Érdekfeszítõ kérdés, mi történik az éppen fekete lyukká alakuló anyag téridõ szerkezetével, esetleg mikroállapotainak számával, amelynek eredményeként az entrópia a felülettel lineáris arányossági kapcsolatra vált át. A fent ismertetett gondolatok abban a megállapításban foglalhatók össze, hogy a gravitációs stabilitás korlátozza a valamely tértartományban tárolható maximális információtartalmat. A termodinamikai, statisztikus fizikai és informatikai entrópiafogalmak összekapcsolódásának felismerése vezethette John Wheelert arra a kijelentésre, hogy a fizika tárgya alapvetõen a Világegyetem fundamentális információtartalmának a feltárása. Ennek ellenére nem várható, hogy a fizikusok elözönlenék a hazai és nemzetközi információtechnológiai pályázatokat. Ugyanis a fenti megállapításoknak a napi haszontermelésnél sokkal izgalmasabb következményei ígérkeznek. G. 't Hooft (6. kép) 1993-ban radikális általánosítását adta Bekenstein észrevételének, amikor a Világegyetem egészét leírni képes, a jövõben megalkotandó elmélet szerkezetére felállította a holografikus elv hipotézist [5], ami azt állítja, hogy a Világegyetem legalapvetõbb független szabadsági fokai kétdimenziós sokaságot alkotnak. Miután óriási tartományról van szó, a határoló felület közelítõen síkkal ábrázolható. A tartomány belsejében zajló folyamatok teljes információtartalma ezen a távoli „vetítõvásznon” elhelyezkedõ szabadsági fokokban rejlõ információval meghatározott, és a határ viselkedésébõl információvesztés nélkül származtatható. 't Hooft párhuzamba állította ezt az elképzelést a háromdimenziós képek kétdimenziós felületen történõ tökéletes kódolásával, a hologrammal. Ennek alapján a fentebb szereplõ entrópiakorlátot holografikus felsõ korlátnak hívják.
Ez a korlát kissé csökkenthetõ, ha feltesszük, hogy a galaxisokba tömörült anyag termikusan tökéletesen szigetelt, azaz a tágulás a mikrohullámú háttérsugárzás lecsatolódása óta adiabatikus. Az akkori, nagyjából ezerszer kisebb tértartomány sugarával számolva a holografikus entrópiakorlát körülbelül milliószorta kisebb a fenti értéknél. A holografikus elv hívei nemcsak egyenlõtlenségként teljesülõ felsõ korlátot, hanem egyenlõséget is remélnek a fenti becslésbõl kiolvasni. Ez pedig csillagászati „vadászatot” indít a hiányzó entrópia nyomában! Egy 2008 júniusában megjelent cikk P.H. Frampton amerikai fizikus tollából azt javasolja, hogy nemcsak szupermasszív fekete lyukak, hanem például a naptömeg ezerszeresét hordozók után is kutatni kellene gravitációs mikrolencse hatásuk felhasználásával. Elegendõ számban az ilyen méretû fekete lyukak jelentõsen hozzájárulhatnának a jelenlegi entrópiatartalmat a holografikus felsõ korláttól elválasztó „szakadék” kitöltéséhez. A történet lezáratlanul vezet a mai részecskefizikai kutatások élvonalába, miután I. Klebanov és L. Susskind, valamint B. Thorn felismerték, hogy a húrelméletnek van olyan megfogalmazása, amely teljes mértékben megfelel 't Hooft várakozásának. Ugyanakkor mindmáig izgalmas vitakérdést jelent, hogy a fundamentális (Planck-hossznyi méretekben releváns) szabadsági fokok számát általában korlátozza-e a holografikus elv. Érdemes megjegyezni, hogy a fekete lyuk felületére koncentrált dinamikai szabadsági fokok feltevésével a fekete lyukak keletkezése és elpárolgása unitér folyamat, azaz a fekete lyukba hulló információ annak felületén tárolódik valamiképpen. Nemrég színpadias gesztussal az információvesztés lehetõségét eredetileg pártoló Hawking vesztesnek nyilvánította magát és átállt a holografikus elvet elfogadók táborába. Zárásként az abszolút fekete test egykori és a fekete lyuk jelenkori tudománytörténeti szerepe közötti párhuzamra hívnám fel a figyelmet. Az abszolút fekete test sugárzásának univerzális jellege lehetõvé tette, hogy Plancknak arra talált kvantumos leírását csakhamar más jelenségkörben fellépõ „oszcillátorokra” is kiterjesszék, néhány évtized alatt kialakuljon a kvantum- természettudomány. Elképzelhetõ, hogy hasonló univerzalitású elméleti keretté épül a tetszõleges objektum által hordozott információ, amely keret jelenlegi megértési szintjét a fekete lyukak entrópiájára alapozott entrópiamaximum tulajdonsága, és az abból kinõtt holografikus elv képviseli.
- M. Planck: Válogatott írások. (szerk. Szegedi Péter) Typotex, Budapest, 2003, 285 oldal.
- S. Varró: Einstein's Fluctuation Formula. A Historical Overview. Fluctuation and Noise Letters (2006) R11-R46.
- J.D. Bekenstein: Black Holes and Entropy. Phys. Rev. D7 (1973) 2333-2346.
- J.D. Bekenstein: Entropy Bounds and Black Hole Remnants. Phys. Rev. D49 (1994) 1912-1921.
- R. Bousso: The Holographic Principle. Rev. Mod. Phys. 74 (2002) 825-874.
___________________
Az MTA Fizikai Osztály és az ELFT által Max Planck születésének 150. évfordulójának tiszteletére rendezett emlékülésen elmondott eloadás írott változata.
 A radioaktivitást 1896-ban Henri Becquerel francia tudós fedezte fel, amiért 1903-ban megkapta a fizikai Nobel-díjat. Becquerel foszforeszkáló anyagokkal kísérletezett. Úgy gondolta, hogy a katódsugárcső fénye valamilyen módon összefügg a foszforeszcenciával. Különféle foszforeszkáló anyagokat burkolt fekete papírba egy fényképlemezzel együtt, és a fényképlemez feketedését vizsgálta. Nem észlelt feketedést amíg uránsókkal nem próbálkozott. Miután a nem foszforeszkáló uránsókkal próbálkozott, kiderült, hogy a jelenségnek semmi köze sincs a foszforeszcenciához. Kimutatta, hogy a sugárzás intenzitása arányos az urán koncentrációjával, így arra következtetett, hogy ez a sugárzás az uránatom tulajdonsága. Pierre és Marie Curie új, sugárzó elemek után kutatva fedezték fel, hogy a tórium is sugároz. Az uránércből kivontak még két erősebben sugárzó elemet, a polóniumot és a rádiumot. A Curie házaspár nehéz és fárasztó munkájának szemléltetéséül: nyolc tonna uránércből 0,1 gramm rádium nyerhető ki. A Curie házaspár és Ernest Rutherford kísérletei a radioaktív sugárzásnak két összetevőjét mutatta ki: a nagyon rövid hatótávolságú (levegőben kevesebb, mint 1 cm) alfa-sugárzás, és a béta-sugárzás (pár 10 cm levegőben). 1900-ban fedezte föl Paul Ulrich Villard a gamma-sugárzást, amit 10 cm ólom sem bír elnyelni. Később bebizonyították, hogy a gamma-sugárzás valójában nagyenergiájú elektromágneses sugárzás.
A radioaktivitást 1896-ban Henri Becquerel francia tudós fedezte fel, amiért 1903-ban megkapta a fizikai Nobel-díjat. Becquerel foszforeszkáló anyagokkal kísérletezett. Úgy gondolta, hogy a katódsugárcső fénye valamilyen módon összefügg a foszforeszcenciával. Különféle foszforeszkáló anyagokat burkolt fekete papírba egy fényképlemezzel együtt, és a fényképlemez feketedését vizsgálta. Nem észlelt feketedést amíg uránsókkal nem próbálkozott. Miután a nem foszforeszkáló uránsókkal próbálkozott, kiderült, hogy a jelenségnek semmi köze sincs a foszforeszcenciához. Kimutatta, hogy a sugárzás intenzitása arányos az urán koncentrációjával, így arra következtetett, hogy ez a sugárzás az uránatom tulajdonsága. Pierre és Marie Curie új, sugárzó elemek után kutatva fedezték fel, hogy a tórium is sugároz. Az uránércből kivontak még két erősebben sugárzó elemet, a polóniumot és a rádiumot. A Curie házaspár nehéz és fárasztó munkájának szemléltetéséül: nyolc tonna uránércből 0,1 gramm rádium nyerhető ki. A Curie házaspár és Ernest Rutherford kísérletei a radioaktív sugárzásnak két összetevőjét mutatta ki: a nagyon rövid hatótávolságú (levegőben kevesebb, mint 1 cm) alfa-sugárzás, és a béta-sugárzás (pár 10 cm levegőben). 1900-ban fedezte föl Paul Ulrich Villard a gamma-sugárzást, amit 10 cm ólom sem bír elnyelni. Később bebizonyították, hogy a gamma-sugárzás valójában nagyenergiájú elektromágneses sugárzás.  A béta-bomlás elméletét az olasz Fermi adta meg 1934-ben. A béta-bomlás során a magban lévő neutron bomlik el protonra és elektronra. A béta részecskék folytonos energia eloszlása azonban azt sugallta, hogy a folyamatra nem teljesül az energia megmaradása. Hogy ez teljesüljön, azt kellett feltenni, hogy egy kistömegű semleges részecske is keletkezik a bomlás során, ami energiát és impulzust visz magával. Ennek a részecskének Fermi a neutrinó nevet adta. A pozitron-sugárzást 1933-ben fedezte fel a Joliot-Curie házaspár. Ennél a folyamatnál az elem rendszáma eggyel csökken egy proton elbomlása miatt, miközben az elektron antirészecskéje, a pozitron keletkezik. Az elektronbefogást az amerikai Alvarez ismerte fel 1937-ben. Ennél a folyamatnál úgy csökken az elem rendszáma, hogy a mag a hozzá legközelebb lévő elektronpályáról befog egy elektront, ami egy protonnal neutronná egyesül.
A béta-bomlás elméletét az olasz Fermi adta meg 1934-ben. A béta-bomlás során a magban lévő neutron bomlik el protonra és elektronra. A béta részecskék folytonos energia eloszlása azonban azt sugallta, hogy a folyamatra nem teljesül az energia megmaradása. Hogy ez teljesüljön, azt kellett feltenni, hogy egy kistömegű semleges részecske is keletkezik a bomlás során, ami energiát és impulzust visz magával. Ennek a részecskének Fermi a neutrinó nevet adta. A pozitron-sugárzást 1933-ben fedezte fel a Joliot-Curie házaspár. Ennél a folyamatnál az elem rendszáma eggyel csökken egy proton elbomlása miatt, miközben az elektron antirészecskéje, a pozitron keletkezik. Az elektronbefogást az amerikai Alvarez ismerte fel 1937-ben. Ennél a folyamatnál úgy csökken az elem rendszáma, hogy a mag a hozzá legközelebb lévő elektronpályáról befog egy elektront, ami egy protonnal neutronná egyesül. 1934: Az első mesterséges radioaktív izotópot, a 30-as tömegszámú foszfort a Joliot-Curieházaspár állította elő. Alumíniumot sugároztak be alfa részecskékkel. Az alfa részecskék neutronokat és pozitronokat löktek ki az alumíniumból. A besugárzást megszüntetve az alumínium pozitront sugárzott ki. (Ők csak valami pozitív sugárzást detektáltak, a pozitront később azonosították. A neutront sem ismerték még ekkor.) A pozitron sugárzás intenzitása a radioaktív bomlásnak megfelelő módon csökkent. Ez utalt arra, hogy radioaktív elem keletkezett. Miután a besugárzott alumíniumban kémiailag kimutatták a foszfor és a szilícium jelenlétét, a folyamat világossá vált.
1934: Az első mesterséges radioaktív izotópot, a 30-as tömegszámú foszfort a Joliot-Curieházaspár állította elő. Alumíniumot sugároztak be alfa részecskékkel. Az alfa részecskék neutronokat és pozitronokat löktek ki az alumíniumból. A besugárzást megszüntetve az alumínium pozitront sugárzott ki. (Ők csak valami pozitív sugárzást detektáltak, a pozitront később azonosították. A neutront sem ismerték még ekkor.) A pozitron sugárzás intenzitása a radioaktív bomlásnak megfelelő módon csökkent. Ez utalt arra, hogy radioaktív elem keletkezett. Miután a besugárzott alumíniumban kémiailag kimutatták a foszfor és a szilícium jelenlétét, a folyamat világossá vált.